Alzheimers sjukdom
Alzheimers sjukdom är den vanligaste förekommande av demenssjukdomarna och hör till de primärdegenerativa sjukdomarna. Det som särskiljer Alzheimers sjukdom från övriga primärdegenerativa sjukdomar är att den initialt drabbar hippocampus och det episodiska närminnet.
Definition av Alzheimers sjukdom
Definitionen av demens är en uttalad kognitiv svikt som påverkar arbete och/eller socialt liv. Den funktion som drabbas är vanligtvis minnet men även visuospatial förmåga, orienteringsförmåga, praktisk förmåga samt språk och exekutiv förmåga påverkas mer eller mindre. Även personlighet inklusive omdömesförmåga kan förändras vid demenssjukdom.
Indelning
Demenssjukdomarna indelas i undergrupper, den vanligaste är de primärdegenerativa sjukdomarna och inom denna är Alzheimers sjukdom vanligast. Andra exempel på primärdegenerativa sjukdomar är fronto-temporal demens (FTD), Lewy-body demens och Demens vid Parkinson samt Huntingtons sjukdom.
Den näst vanligaste demenssjukdomen är vaskulärdemens (VaD), eller blodkärlsrelaterad demenssjukdom.
Man definierar även en grupp sekundära demenssjukdomar där den kognitiva svikten orsakas av en annan typ av sjukdom. Exempel på detta är hjärntumörer i främre och temporala delarna av hjärnan eller infektioner i hjärnan, till exempel HIV, Lues och Creutzfeld-Jacobs sjukdom. Depression hos äldre kan ibland ge kognitiva störningar och likna demens. Även ogynnsam inverkan av läkemedel kan leda till kognitiv svikt och likna demens.
Enkätundersökning om förskrivningspraxis
Den här enkäten riktar sig till dig som är läkare och syftar till att undersöka vilka faktorer som påverkar dina beslut om förskrivning av läkemedel. Vi vill förstå hur sådant som journalsystem, patientpreferenser och ekonomiska överväganden påverkar dina val.
Bakgrund och epidemiologi
Alzheimers sjukdom beskrevs första gången 1906 av den tyska psykiatrikern och patologen Alois Alzheimer. Han redogjorde för ett fall där han kopplade ihop den kliniska bilden med de hjärnförändringar han fann vid en senare hjärnobduktion. Vid detta tillfälle beskrev han för första gången de för Alzheimers sjukdom typiska förändringarna, nämligen atrofi av hjärnan samt förekomst av tangles (nystan) och plack (korn).
Det finns ett stort antal tillstånd och sjukdomar som leder till kognitiv svikt och demens. Alzheimers sjukdom är vanligast och cirka 60–70 procent av alla som får en demensdiagnos lider av Alzheimers sjukdom. Sjukdomen är starkt relaterad till ålder på så sätt att cirka 30–40 procent av alla personer över 85–90 år drabbas av sjukdomen, medan den är mycket ovanlig under 60 år.
Vi räknar med att det finns ungefär 85 000 personer med Alzheimers sjukdom i Sverige och att upp till 12 000 personer insjuknar varje år. Den totala kostnaden för all demensvård och omvårdnad uppgår till mer än 65 miljarder kronor per år. Den fördelas ojämnt på så sätt att majoriteten av kostnaden ligger inom den primärkommunala verksamheten och endast cirka fem procent ligger inom regionernas verksamheter.
Det anses att sjukdomen i sig förkortar den sjukes förväntade liv, och denne avlider i genomsnitt cirka tio år efter diagnos. Vanligtvis i någon form av infektionssjukdom, till exempel lunginflammation eller urinvägsinfektion.
Etiologi och patogenes
Kunskapen kring hur sjukdomen uppstår och utvecklas har ökat väsentligt de senaste tio till femton åren. Bakgrunden är bland annat att man har kunnat studera vissa ovanliga ärftliga former som beror på mutationer, överfört dessa mutationer till djurmodeller och på sätt ökat kunskapen kring patogenes och etiologi. Det har också under senare år blivit tydligt att Alzheimer har en mer komplex bakgrund än vad man tidigare ansett. Det finns en koppling mellan sjukdomen och livsstil, man har till exempel identifierat en rad risk- och skyddsfaktorer kopplat till sjukdomens utveckling.
Vi vet dock i princip inte varför sjukdomen uppstår. Undantaget är det mycket sällsynta fall där sjukdomen beror på en mutation i arvsmassan. Det finns beskrivet ett flertal mutationer, bland annat i APP-genen (amyloid percursor protein) och i presenil 1 respektive 2 generna. I dessa fall drabbas de sjuka tidigt i livet, mellan 40 och 60 år, sjukdomen är autosomalt dominant och har mycket hög penetrans, närmare 100 procent. I dessa fall orsakas sjukdomen av en överproduktion av ett ämne som kallas betaamyloid, vilket är ett 42 aminosyror långt protein vars funktion för närvarande inte är känd. Knappt en procent av samtliga Alzheimerfall i världen anses bero på dessa mutationer.
Den dominerande typen av Alzheimers sjukdom är de sporadiska fallen och i dessa fall vet vi ännu inte varför sjukdomen uppstår. Forskare har dock föreslagit en hypotes; amyloid-hypotesen, vilken innebär att man kopplar ihop sjukdomens utveckling med en överproduktion av nyss nämnda betaamyloidproteinet. Betaamyloid återfinns i placken som beskrevs av Alzheimer, och placken återfinns extracellulärt i hjärnan. Den andra patologiska förändring han beskrev; tangles, består av sammanfallet stödjeprotein i nervcellerna och destruktion av dessa strukturer beror på ett förändrat tauprotein.
Det finns evidens för att betaamyloid i protofibrillformer, det vill säga korta lösliga proteinkedjor, utövar en stark giftverkan på nervcellerna. Som sekundära fenomen anses senare ske en förändring av tauproteinfunktionen och till slut en accelererande nervcellsstöd.
Det finns en stark koppling mellan symtomutvecklingen av sjukdomen och tangles i hjärnan. Den del av hjärnan som först drabbas är entorhinalcortex i mediala temporalloberna, senare afficieras närliggande strukturer såsom hippocampus, övriga delar av temporallober och hjässlober och slutligen även frontalloberna. Vissa delar av hjärnan blir nästan aldrig påverkade, som till exempel motor- och premotorcortex liksom lillhjärnan. Orsaken till denna selektivitet är inte känd.
Amyloidhypotesen har under senare tid ifrågasatts som enda förklaring till sjukdomen då man i ett stort antal läkemedelsstudier inte haft framgång med läkemedel som påverkar amyloiden i hjärnan. Troligtvis är sjukdomen mer komplex och flera faktorer, till exempel kärlförändringar, spelar troligen roll.
Det finns en rad riskfaktorer kopplade till utvecklingen av Alzheimers sjukdom. Förutom ärftlighet är exempelvis kvinnligt kön en riskfaktor, orsaken till detta är inte känt. Som tidigare nämnts kan sjukdomen ibland förekomma som följd av mutationer. Det finns ytterligare en ärftlig faktor och det är förekomst av riskgenen ApoE4.
ApoE är ett protein som transporterar fett. Den förekommer i tre isoformer: ε 2, ε 3 och ε 4 och personer med ε 4 har en ökad riska att insjukna. Om man har en allel ε 4 ökar risken tre till fyra gånger och har man två alleler ökar risken med åtta till tio gånger. Den exakta mekanismen för ApoE:s roll i hur Alzheimer uppstår är inte känd.
Vissa livsstilsfaktorer har kunnat kopplas till utveckling av Alzheimers sjukdom. Till exempel vet vi att högt blodtryck och höga blodfetter i medelåldern kan utgöra en risk för att 20–30 år senare insjukna i Alzheimers sjukdom. Faktorer såsom mental stimulering och fysisk aktivitet tycks utgöra skyddande faktorer mot sjukdomen. Andra riskfaktorer är diabetes typ 2, övervikt och alkoholöverkonsumtion.
Födoämnesrelaterade faktorer har visat sig ha skyddande effekt. Till exempel kan fleromättade fetter (särskilt omega-3) i exempelvis fisk utgöra en skyddande faktor. Det finns också en koppling till vitamin B12 och folsyra på så sätt att hos Alzheimersjuka hittas ofta låga värden/ brist på dessa vitaminer. Men man har hittills inte vid någon interventionsstudie lyckats förbättra den kognitiva funktionen med hjälp av B12-eller folsyrabehandling.
Klinisk bild av Alzheimers sjukdom
De första symtomen utgörs av en, långsamt debuterande smygande minnesstörning – till en början en episodisk närminnesstörning. Så småningom tillkommer andra kognitiva brister, till exempel oförmåga att hitta i omgivningarna, en ökad oförmåga att använda händerna på ett ändamålsenligt sätt (dyspraxi) samt en visuospatial oförmåga. Ett symtom som kommer tidigt är dysexekutiv förmåga, vilket innebär svårighet att på ett ändamålsenligt sätt processa och reagera på information, vilket av omgivningen ofta uppfattas som passivitet och ointresse.
Den kognitiva funktionsnedsättningen fortskrider långsamt, det kan ta ett flertal år innan den drabbade söker läkare och härefter kan sjukdomsprocessen pågå ytterligare åtta till tio år med en alltmer påtaglig kognitiv störning. Så småningom förloras alltmer minnesmaterial och det innebär att också mycket av det självbiografiska minnet går förlorat. Personer med en avancerad Alzheimerdemens lever därmed många gånger i den tid där de själva har minnesmaterial, det kan röra sig om 30–40 år tillbaka i tiden. I samband med den kognitiva funktionsnedsättningen ökar behovet av hjälp från omgivningen. I slutstadierna blir patienterna helt hjälpberoende, oftast har de helt tappat sitt språk och kommunikationen till anhöriga och vårdgivare är i stort sett bruten.
Många Alzheimersjuka minskar i vikt på ett oförklarligt sätt. Det skulle delvis kunna förklaras med att man så småningom tappar luktsinnet och därmed smak och att detta påverkar aptiten. En ökad dyspraxi då det gäller ätande kan också spela roll. Den tilltagande kakexin leder sannolikt till ökad infektionskänslighet, men om det är enda förklaringen bakom ökad infektionskänslighet är inte känt. Som tidigare nämnts avlider patienterna vanligtvis i lunginflammation eller urinvägsinfektion.
Under sjukdomsförloppet är det vanligt med psykiatriska och beteendemässiga komplikationer. Tidigt i sjukdomen då insikten är opåverkad förekommer perioder av depression och nedstämdhet. Även ångest förekommer i samband med sjukdomsdebuten och i synnerhet då diagnos meddelas. Så småningom kan det utvecklas paranoida vanföreställningar liksom andra typer av vanföreställningar och psykotiska symtom i form av syn-, hörsel- eller känselhallucinationer.
Beteendestörningar i form av aggressivitet, irritabilitet, sömnstörning och vandringsbeteende kan också förekomma och utgör då en stor belastning för anhöriga och vårdgivare. Dessa perioder med psykiatriska beteendemässiga symtom varierar under sjukdomsförloppet och i princip går de alltid över, men kan komma på nytt och då i andra former.
Diagnostik
Diagnosen Alzheimers sjukdom ställs med hjälp av diagnostiska kriterier som beskrivs i DSM-IV, DSM-5 och ICD-10. Dessa kriterier baseras på symtombild och är inte kopplade till någon form av patogenetiskt resonemang. För att få diagnosen Alzheimers demens krävs en omfattande kognitiv störning (så omfattande att arbete eller socialt liv påverkas) där minnesstörningen ska dominera. Information om detta fås genom en noggrant strukturerad intervju av närstående eller vårdgivare.
Nya modifierade diagnostiska kriterier har föreslagits i DSM-5. Man talar i DSM-5 om kognitiv sjukdom och lindrig kognitiv funktionsnedsättning i stället för demens och kognitiv svikt.
I DSM-5 blir det då kognitiv sjukdom av Alzheimer typ, eller kognitiv sjukdom beroende på Alzheimers sjukdom.
Det finns nu nya publicerade kriterier (Dubois kriterier, International Working Group for Alzheimers disease, IWG) som är mer baserade på de bakomliggande patogenetiska mekanismerna, dessa är under utveckling och testas i olika kliniska sammanhang. Detta sätt att diagnosticera Alzheimer kommer sannolikt att ändra diagnoskriterierna i en snar framtid.
Demensutredning
Denna ska ske enligt socialstyrelsens uppdaterade riktlinjer från 2017.
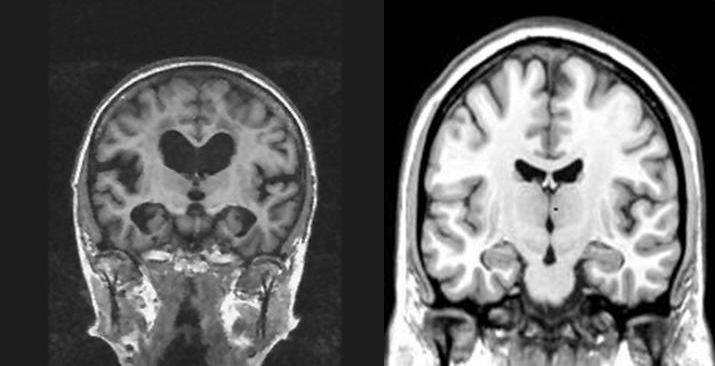
Basen i en demensutredning är anamnes och status och i status ska en noggrann psykiatrisk och neurologisk undersökning utföras förutom sedvanlig somatisk status. Till hjälp vid utredningen finns neuroradiologisk undersökning; datortomografi eller magnetkamera. Här vill man få en uppfattning om det förekommer en lokaliserad och/eller generell atrofi av hjärnan. Till de tidigaste tecknen på Alzheimers sjukdom hör atrofi av mediala temporalloberna vilket kan ses både vid CT och MR. Information om förekomst av kärlskador är också differentialdiagnostiskt värdefullt.
En annan möjlighet är att studera regional cerebral glukosomsättning i hjärnan med hjälp av PET (positron emission tomography) och här är de typiska förändringarna en nedsättning av sockeromsättningen temporalt och parietalt. På senare tid har man börjat använda specifika diagnostiska markörer med hjälp av PET då man tillför ett ämne som specifikt fäster vid beta-amyloid och plack och sedan ger ifrån sig en positronstrålning som kan registreras. Även avbildning av tau-proteinet är under utveckling. Dessa metoder är fortfarande under utveckling men kommer ha stor betydelse i framtiden.
En annan viktig diagnostisk metod är att studera de specifika proteinförändringar som finns i lumbalvätskan, vilket sker genom en vanlig lumbalpunktion och analys av CSF-vätskan avseende tau, hyperfosforerat tau och betaamyloid. Typiskt mönster vid Alzheimer är att betaamyloid sänks och att tau och hyperfosforerat tau ökar. Under senare tid har man utvecklat metoder att analysera bland annat tau-proteiner i blod. När detta blir kliniskt användbart kommer det innebära en stor förändring i det diagnostiska arbetet.
Då det gäller andra blodanalyser bör man få en uppfattning om det förekommer bakomliggande sjukdomar, vilka kan försämra den kognitiva funktionen. Man måste därför utesluta förändringar i tyreoidea och paratyreoideafunktion, liksom få en uppfattning om B12- och folsyrabrist föreligger. Därför rekommenderas TSH och kalcium samt homocystein som markör för B12- och folsyrabrist.
I en demensutredning skall det också ingå en undersökning av patientens funktion i det vardagliga livet och denna undersökning bör göras systematiskt, till exempel av en arbetsterapeut. Information om hur patienten klarar sig, om han eller hon kan sköta sin egen hygien, klara matlagning, klä på sig etcetera är ett måste.
Differentialdiagnoser
Det är svårt att diagnostisera Alzheimers sjukdom tidigt i sjukdomsförloppet. På grund av svagheter i de nuvarande diagnostiska kriterierna har man tidigare infört begreppet MCI (mild cognitive impairment) eller ”lindrig kognitiv störning”, i DSM-5, lindrig kognitiv nedsättning. Detta begrepp innebär objektiva och/eller subjektiva tecken på minnesstörning, men även annan kognitiv störning kan förekomma. Störningen är dock inte så uttalad att det påverkar det alldagliga livet eller arbetet. Alltså kan man definitionsmässigt inte ställa en demensdiagnos. En Alzheimers sjukdom debuterar alltid som en MCI-patient och först när den kognitiva störningen är uttalad ställs diagnosen Alzheimers demens.
Av andra demenssjukdomar kan Lewy body demens och i tidiga skeden även frontallobsdemens likna Alzheimers sjukdom, men den kliniska bilden blir oftast tydlig om man gör en noggrann anamnes och ett noggrant status. Ett bra hjälpmedel i differentialdiagnostiska sammanhang då det gäller Lewy body demens är att använda en SPECT-metod för att mäta dopamintransportersystemet i hjärnan. Demens orsakad av Lewy body (Lewy body demens och demens vid Parkinsons sjukdom) har reducerad dopaminaktivitet i basala ganglierna jämfört med Alzheimers sjukdom.
Vaskulär demens är en annan differentialdiagnos som i sin tydligaste form inte behöver vara särskilt komplicerad att skilja från Alzheimer. Om vaskulär demens emellertid beror på så kallad småkärlssjuka kan det ibland vara svårt att särskilja de bägge tillstånden. Det är också vanligt att Alzheimers sjukdom och cerebrovaskulär hjärnskada förekommer samtidigt vilket kan komplicera bilden. Om man vid en hjärnscanning (MR eller CT) finner tecken på cerebrovaskulär hjärnskada, till exempel vitsubstansskador och enstaka lakunära infarkter, och om man samtidigt har en typisk klinisk Alzheimerbild bör man sätta diagnosen blanddemens.
Tidiga fall av depression med kognitiv svikt/läkemedelspåverkan med kognitiv svikt kan också likna en tidig Alzheimer, vilket man bör vara medveten om. I många av dessa fall kan lumbalpunktion och/eller MR/CT vara till hjälp för att studera mediala temporallober. Finner man normala likvoranalyser och inga förändringar på MR/CT talar det starkt emot Alzheimers sjukdom.
Behandling
Farmakologisk behandling vid Alzheimers sjukdom
Det finns för närvarande symtomlindrande behandling i form av acetylkolinesterashämning och farmakologisk påverkan på glutamatsystemet i hjärnan.
Acetylkolinesterashämning har effekt därför att det tidigt i sjukdomsförloppet sker en nedsättning av de acetylkolinerga funktionerna i hjärnan. Det finns tre preparat; donepezil, galantamin och rivastigmin vilka samtliga har liknande kliniska effekter. De skiljer sig något åt då det gäller biverkan. Dosering och biverkan enligt tabell 1 nedan.
Den andra typen av farmakologisk behandling är glutamataktivitetsreglering genom memantin. Memantin är registrerat för måttlig till svår Alzheimer.
Generellt gäller att man ska titrera in medicinen långsamt vilket reducerar biverkningsrisken. Innan man sätter in acetylkolinesterashämmare bör ett EKG kontrolleras för att utesluta överledningsrubbning. Patienter med astma ska också behandlas med försiktighet. Indikationen för behandling med acetylkolinesterashämmare är mild till måttligt svår Alzheimers sjukdom. Det finns numera också data som tyder på effekt vid svår Alzheimers sjukdom.
De vanligaste biverkningarna vid kolinesterashämmare är gastrointestinala med illamående, kräkningar och diarréer. Överledningsrubbningar förekommer också. Vid behandling med memantin är huvudvärk och yrsel de vanligaste biverkningarna. Rivastigmin finns nu också som plåster vilket reducerar de gastrointestinala biverkningarna.
Patientens och anhörigas välbefinnande
Förutom farmakologisk behandling måste insatser göras för patientens och anhörigas välbefinnande. Det är viktigt med saklig upplysning både till patient och anhöriga i samband med att diagnos meddelas. Uppföljning, gärna kort efter diagnosmeddelandet, är viktigt för att förebygga fördjupade krisreaktioner.
Erfarenhetsmässigt mår anhöriga och patient bra av att få diskutera sjukdom och prognos i lugn och ro några veckor till månader efter att diagnosen meddelats. I detta sammanhang kommer ofta frågor om ärftlighet upp och bör också diskuteras på ett sakligt sätt. Vid misstanke om starkt ärftliga komponenter kan man också hänvisa till klinisk genetiska rådgivningsenheter.
Alzheimersjuka kan många gånger bo kvar länge i hemmet med stöd och hjälp av anhöriga och av kommunen. Stöd och hjälp i hemmet kan många gånger ges i resten av patientens liv. Kan den sjuke inte längre bo kvar hemma finns möjlighet till särskilt boende i gruppboende eller sjukhem.
Nationella riktlinjer
Det finns numera nationella riktlinjer för vård och omsorg vid demenssjukdom i vilka utredning, behandling och omvårdnad vid Alzheimers sjukdom finns presenterat på ett evidensbaserat sätt. Den senaste reviderade upplagan kom 2017.
Tabell 1: Farmakologisk behandling av Alzheimers sjukdom |
||||
|
Donepezil |
Galantamin Reminyl |
Rivastigmin* Exelon |
Memantin Ebixa |
|
| Indikation |
Lätt–måttlig |
Lätt–måttlig |
Lätt–måttlig |
Måttlig–svår AD |
| Dosering | 1x1 | 1x1 eller 1x2 | 1x2 | 1x1 |
| Dostitrering | Ja: 5–10 mg | Ja: 8–16–24 mg | Ja: 3–6–9–12 mg | Ja: 5–10–15– 20 mg |
| Vanligaste dos | 5 mg | 16 mg | 6–9 mg | 20 mg |
| Vanligaste biverkan | Illamående, kräkningar och diarré | Illamående, kräkningar och diarré | Illamående, kräkningar och diarré | Huvudvärk och yrsel |
*Finns som plåster i doserna 4,6 mg/dygn samt 9,5 mg/dygn (se Fass)
Prognos
Prognosen är för närvarande dyster, det finns ingen bot mot sjukdomen däremot symtomlindrande farmakologisk behandling. Alzheimer har ett långt och långsamt förlopp och patienten blir alltmer beroende av andra i och med att den kognitiva svikten utvecklas. Medelöverlevnad från diagnos är cirka tio år med mycket stor variation. De tidigt debuterande fallen (< 60 år) liksom de hereditära formerna har oftast ett snabbare förlopp jämfört med de sporadiska och sent debuterande. Först då ett sjukdomsmodifierande läkemedel blir tillgängligt kommer prognosen kunna förbättras, i synnerhet om samtidigt diagnostiken förbättras.
Komplikationer
Under sjukdomsförloppet förekommer som tidigare nämnts ofta psykiatriska och beteendemässiga förändringar (BPSD = beteendemässiga och psykiska symtom vid demenssjukdom). Dessa utgörs av ångest, oro, sömnstörningar, psykotiska symtom såsom hallucinationer och vanföreställningar samt depressiva symtom. Motorisk oro, rop- och vandringsbeteende samt aggressivitet är andra exempel på BPSD. Symtombilden varierar under hela sjukdomsförloppet och i början dominerar ångest och depressiva symtom. Under senare delen av sjukdomen uppträder psykotiska symtom samt motorisk oro mer frekvent.
Särskilda och/eller förebyggande råd
Numera anses kontroll av högt blodtryck och höga blodfetter i medelåldern kunna förebygga senare utveckling av Alzheimer. En kost med riklig förekomst av fleromättade fetter (särskilt omega-3 fetter) anses också kunna motverka en utveckling av sjukdomen, men mer forskning behövs för att mer i detalj studera mekanismerna bakom detta. Fysisk och mental aktivitet samt sociala kontakter är andra skyddande faktorer.
Vidare information
Bilder av Alzheimers sjukdom och hjärnan
Nationella riktlinjer för vård och omsorg vid demenssjukdom, Socialstyrelsen
Behandlingsrekommendationer, Läkemedelsverket
Alzheimers sjukdom på eMedicine
ICD-10
F00.0* G30.0† - Demens vid Alzheimer’s sjukdom, tidig debut
F00.1* G30.1† - Demens vid Alzheimer’s sjukdom, sen debut
F00.2* G30.8† - Demens vid Alzheimer’s sjukdom, atypisk eller blandad typ
F00.9* G30.9 † Demens vid Alzheimer’s sjukdom, ospecificerad
Referenser
- Nationella Riktlinjer för vård och omsorg vid demenssjukdom, Socialstyrelsen 2017.
- Norberg A. Alzheimers sjukdom, Studentlitteratur 2013
-
Marcusson, Blennow, Skoog och Wallin Demenssjukdomar Liber förlag 2011
-
Basun med flera, Boken om demenssjukdomar 2013
-
Nilsson, Wallin, Wahlund, Kognitiv Medicin, Studentlitteratur 2011
-
Wahlund med flera, Geriatrikboken Liber förlag 2020