Claudicatio intermittens (CI) – benartärsjukdom
Benartärsjukdom (PAD, Peripheral Arterial Disease eller PAOD, Peripheral Arterial Occlusive Disease) är en följd av otillräcklig blodcirkulation i benens artärer, vilket leder till en kronisk eller akut ischemi i de nedre extremiteternas vävnader.
Indelning
Benartärsjukdom kan delas in i claudicatio intermittens (CI)/”fönstertittarsjuka” och i kritisk ischemi.
- Claudicatio intermittens definieras som reproducerbar och övergående ischemisk muskelvärk.
- Kritisk ischemi innefattar nattlig vilovärk, vilosmärta och/eller sår och gangrän.
I det följande kommer endast cludicatio intermittens att beröras. (För en vetenskapligt exaktare definition och indelning hänvisas till TASC II-dokumentet.)
Bakgrund och epidemiologi
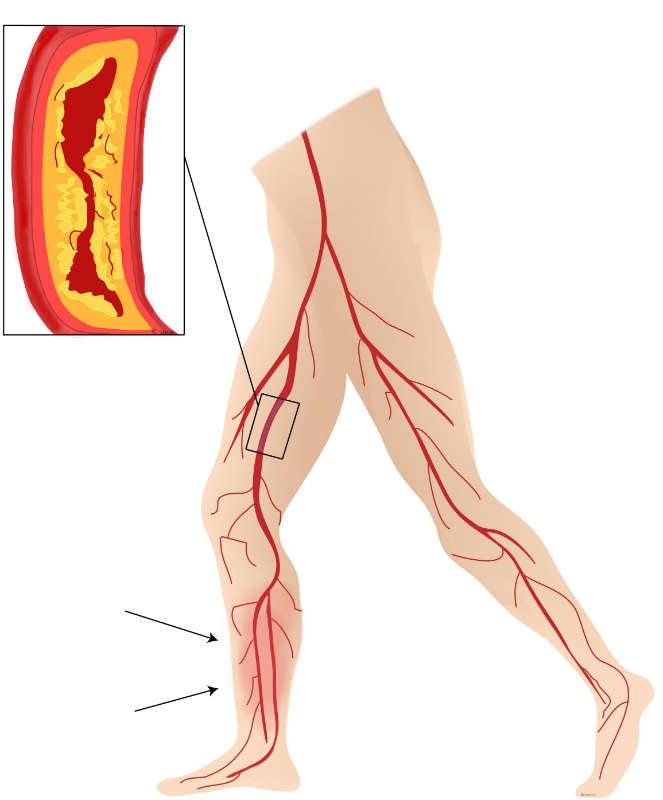
Benartärsjukdom beror till helt övervägande del på ateroskleros vilket medför förträngningar i benens artärer. Den blodflödesbegränsande effekten av stenoserna ger upphov till underperfusion av muskulatur och andra vävnader, vilket medför symtom som är relaterade till ansträngning. (Bild 1)
Prevalens
Prevalensen av symtomatisk CI har i amerikanska material angivits vara 1,3 procent i åldersgruppen 40–59 år, 4 procent i åldersgruppen 60–69 år och 10 procent vid ålder över 70 år. I ett svenskt material rapporterades en kronisk symtomgivande benartärsjukdom hos 4,1 procent av dem i åldersgruppen 50–89 år, medan prevalensen i en tysk studie bland primärvårdspatienter över 65 år var 19,8 procent hos män och 16,8 procent hos kvinnor.
Det uppskattas att cirka 10–20 procent av alla pensionärer i Sverige har någon form av benartärsjukdom och det görs drygt 5000 ingrepp årligen för detta tillstånd, vilket motsvarar cirka 600 ingrepp per miljon invånare och år.
Incidens
Det finns inga tillförlitliga incidenssiffror för CI.
Mortalitet
Mortaliteten är cirka 10-15 procent efter fem år och till 75 procent är den relaterad till kardiovaskulära orsaker.
Flera riskfaktorer avgör hypotermi vid operation
Lär dig mer om perioperativ hypotermi genom NetdoktorPros webbaserade utbildning.
Etiologi och patogenes
Ateroskleros innebär inlagringar av fetter i kärlväggen och initiering av en inflammatorisk process som medför kalcifikation och plackbildning. Dessa aterosklerotiska plack leder till en lumeninskränkning i artären med åtföljande hämning av blodflödet om lumendiametern understiger 50 procent. Detaljerna i åderförkalkningsprocessen är fortfarande inte helt klarlagda, men till riskfaktorerna som påverkar aterosklerosen negativt räknas:
- Rökning; helt dominerande riskfaktor
- Diabetes mellitus
- Hypertoni
- Hyperlipidemi
- Inaktivitet och nedsatt rörlighet
- Övervikt
- Kön, män är överrepresenterade
Klinisk bild
Den kliniska bilden av CI kännetecknas av att patienten söker för smärtor i benen som ökar i takt med ansträngningen och släpper i vila. Oftast är besvären ensidiga eller med övervikt till en sida. Klassiskt anges krampliknande smärtor ”som vid mjölksyra” i vadmuskulaturen vid gång och som tilltar med gångsträckan, men som snabbt avtar och försvinner i vila varefter promenaden kan fortsätta – härav namnet fönstertittarsjuka, claudicatio intermittens, tillfällig hälta. Just det snabba avklingandet av besvären i vila är kännetecknande för den övergående ischemin vid CI och skall alltid efterfrågas anamnestiskt.
Besvären kan också vara lokaliserade till lår- och sätesmuskulaturen. Härvid står smärtorna i bakgrunden och patienten klagar mer över en kraftlöshet och trötthet i benen (domningar), framför allt vid trappstigning och gång i branta backar.
Besvären är relativt monotona i den bemärkelsen att de är likartade och med en väsentligen oförändrad gångsträcka från gång till gång. Fluktuationer över tiden kan dock anges, liksom att gångsträckan efter den första pausen blir längre än vad den var initialt (så kallad ischemisk betingning).
Svullnad, sårbildning och nattliga smärtor eller kramper hör inte till den kliniska bilden vid CI.
Diagnostik
Anamnesen är, som vid alla sjukdomar, viktig. Vid perifer kärlsjukdom är den dock av avgörande betydelse då redan en rätt utförd anamnes kan ge upplysning över var stenosen/ocklusionen sitter och därmed behandlingsmöjlighet och -indikation. Det är viktigt att efterfråga den maximala gångsträckans längd, alltså tills patienten får så ont att denne måste stanna. Sträckan till smärtdebut kan variera betydligt och vara individuellt olika, medan den maximala gångsträckan varierar mindre från gång till gång. Besvären är relaterade till graden av ansträngning – ju fortare gång, desto kortare gångsträcka.
Man efterfrågar också vad patienten gör när han inte längre kan gå och vad som då händer med smärtorna. Om smärtorna snabbt avtar eller försvinner när patienten stannar eller inom någon eller några minuter, talar detta starkt för en cirkulationsrelaterad ischemi. Ett långdraget utebbande av smärtorna över tio till femton minuter, eventuellt i kombination med att behöva sitta på huk eller på en bänk, talar mer för nervrotskompression eller en spinal stenos som upphov till besvären. Smärtor som ökar efter promenaden och som kvarstår länge, kanske till och med ökar i vila hemma i fåtöljen, talar mer för artrosbesvär.
Fråga alltså alltid efter:
- Lokalisation av besvär/smärta
- Maximal gångsträcka
- Vad som händer med besvären/smärtorna vid vila
Enkätundersökning om förskrivningspraxis
Den här enkäten riktar sig till dig som är läkare och syftar till att undersöka vilka faktorer som påverkar dina beslut om förskrivning av läkemedel. Vi vill förstå hur sådant som journalsystem, patientpreferenser och ekonomiska överväganden påverkar dina val.
Undersökningen innefattar inspektion, palpation, auskultation och tryckmätning:
Inspektera
Vid enbart CI-symtom finns inga synliga förändringar, men inspektionen kan avslöja detaljer viktiga för differentialdiagnostiken (exempelvis djup venös insufficiens).
Pulspalpation
Pulsar skall palperas i ljumske, poplitea och på foten (fotrygg för a dorsalis pedis respektive bakom mediala malleolen för a tibialis posterior). Ljumskpulsen brukar sällan vara svårpalperad om den finns, medan popliteapulsen kan vara svårpalperad även i normala fall. Lättast palperas a poplitea bimanuellt vid lätt passivt flekterad knäled relativt proximalt och djupt i fossa poplitea. Pulsen är i sin kvalitet mer indirekt än i ljumsken.
Auskultation
Blåsljud i a iliaca efterforskas genom bilateral auskultation ovan ljumsken mot naveln. Blåsljud i a femoralis kan lätt höras om stetoskopet placeras över den palpabla ljumskpulsen.
Tryckmätning
Ankeltrycksmätning är ett enkelt sätt att dokumentera graden av den arteriella insufficiensen. En blodtrycksmanschett placeras omedelbart proximalt om malleolerna. Med en handdoppler uppsöks flödessignalen från a dorsalis pedis eller a tibialis posterior varefter manschetten blåses upp tills flödesljudet försvinner. Manschetten deflateras och trycket vid återkomst av flödesljudet noteras. Tricket här är att hålla dopplerproben stilla medan manschetten blåses upp – titta på manometern först när flödesljudet hörs. Det högsta uppmätta trycket i de båda fotkärlen noteras.
Ett armtryck tas genom att placera blodtrycksmanschetten på höger överarm medan a radialis auskulteras med dopplerproben vid handleden. Ankeltrycket divideras med armtrycket och ger därmed ABI, ankel-arm index. Normalt ligger detta kring 1,1 – det vill säga ankeltrycket är något högre än armtrycket.
Definitionsmässigt föreligger perifer kärlsjukdom vid ett ABI på 0,9. Som tumregel kan anges att ett ABI på 0,5 ofta ses vid CI, medan vilovärk och gangränrisk korrelerar med ABI på 0,3 respektive 0,2. Det måste dock poängteras att de uppgivna gränserna enbart är ungefärliga riktlinjer – högre ABI kan noteras utan att detta motbevisar en CI. Vid kraftigt förkalkade kärl kan dessa inte komprimeras av blodtrycksmanschetten och falskt höga tryck långt över det systoliska uppmäts. Diabetiker har ibland en mediaskleros vilket gör artärerna svårkompressibla med falskt höga ankeltryck som följd, varför ABI-mätning hos dessa patienter måste värderas kritiskt.
Ibland kan en ganska entydig anamnes inte verifieras med ankeltrycksmätning. Då kan den upprepas efter ett provokationstest med (10)–20 knäböjningar. Det ökade blodflödet efter muskelansträngning kan då demaskera en arteriell stenos som inte är signifikant i vila. ABI blir då klart lägre efter provokationen och framför allt gäller detta vid stenoser i det iliacala kärlområdet.
Först när det står klart att intervention är aktuell (efter riskfaktorbehandling och framgångslös gångträning osv) är det dags att gå vidare med ytterligare kartläggning. Flera alternativ står till buds:
-
MRA: MR-angiografi med magnetresonansteknik. Ger en bra kartläggning av artärsystemet från aorta till foten. Inte alltid tillgänglig vid alla sjukhus. Kan inte utföras på njurinsufficienta patienter (GFR<30 ml/min). Tidigare stentinläggningar medför kraftiga artefakter.
-
CTA: CT-angio med datortomografisk teknik. Ger bra kartläggning av artärerena från aorta till foten. Kalkinlagringar i kärlväggen kan dock störa kraftigt. Stor försiktighet vid njurinsufficienta patienter med förhöjt kreatinin.
-
Angiografi: Konventionell kateterledd kartläggning av artärsystemet med hjälp av jodkontrast. Invasiv diagnostik. Kan i förlängningen övergå direkt i en interventionell endovaskulär åtgärd vid påvisandet av signifikanta stenoser. Försiktighet vid njurinsufficienta patienter.
-
UL: Ultraljudsundersökning med duplexteknik. Nonvinvasiv. Inga kontraindikationer, men undersökarberoende. Oftast mindre lämplig för kartläggning distalt om knäet.
Av dessa undersökningar tycks MRA vara något av en föstahandsmetod då den noninvasivt ger en god överblick av artärsystemet till benen.
Differentialdiagnoser
Listan på tänkbara differentialdiagnoser kan göras lång, men de viktigaste är:
- Venös claudicatio
- Spinal stenos
- Nervrotskompression
- Artros
- Perifer neuropati-neuralgi
- Kroniskt kompartmentsyndrom
- Thrombangiitis obliterans (Mb Buerger)
- Coarctatio aortae
Behandling
Behandlingen vid CI är till helt övervägande del ”konservativ”, det vill säga icke-operativ.
Orsaken till detta är att invasiva rekonstruktiva ingrepp alltid är förenade med risker för ocklusion och därmed försämring av tillståndet, vilket vid en så pass ”lindrig” åkomma som CI kan vara deletärt. Därför bör alltid konservativ handläggning provas i åtminstone tre till sex månader innan det beslutas om fortsatt utredning syftande till intervention.
Då CI till så övervägande del är aterosklerotiskt betingad bör riskfaktorer förknippade med denna bekämpas:
- Rökstopp!
- Acceptabel diabeteskontroll?
- Lipidsänkning? (Statiner 40–80 mg x1)
- Livsstilsförändring (ökad motion; viktminskning; matvanor)?
- Trombocytaggregationshämmare? (Acetylsalicylsyra, exempelvis Trombyl® 75–160 mg x1, eller clopidogrel, Plavix® 75 mg x1)
Behandling med trombocythämmare riktar sig inte i första hand mot CI, utan sker som led i den allmänna aterosklerosbehandlingen för att minska risken för kardiovaskulära händelser.
Gångträning
En mer specifik behandling mot CI är gångträning. Minst tre till fyra gånger per vecka (och 30 minuter åt gången) promenad till eller över smärtgränsen, det vill säga till den maximala gångsträckan. Därefter vila och upprepning. Information om hur gångträningen skall bedrivas (systematiskt, regelbundet) är viktig – alltför många patienter har bara fått allmänna råd om att ”gå mera” (se även www.fyss.se). Det är viktigt att informera om att träningsutlöst smärta inte kan ge gangrän, att sjukdomen inte försämras av träning och att risken för amputation är liten. Systematisk, helst övervakad, gångträning har visat sig resultera i samma gångsträcka efter två år som efter invasiva endovaskulära åtgärder. Träningen skall bedrivas minst tre månader innan effekten utvärderas.
Sedan 2008 finns ett läkemedel registrerat för behandling av CI, cilostazol (Pletal® ), som kan öka gångsträckan hos utvalda patienter. Cilosatazol är en fosfodiesterashämmare med vasodilaterande och (reversibelt) trombocythämmande effekt, men den exakta verksamhetsmekanismen på besvären vid CI är inte helt klarlagda. Erfarenheterna av preparatet är ännu begränsade, men kan vara ett alternativ till intervention om gångträning och modern sekundärprofylaktisk behandling inte lett till förbättring.
Interventionsindikationer
Vid gravt invalidiserande (det vill säga kraftigt livsföringsinskränkande) CI, trots adekvat riskfaktorsanering och gångträning i minst tre månader, kan kärlintervention övervägas. Här är det inte gångsträckebegränsningen i absoluta antal meter som är utslagsgivande, utan mera graden av patientens upplevda inskränkning av livsföringen. Gränsen för svår eller lindrig–måttlig CI har angetts till under eller över cirka 150 meter.
För val av tidpunkt och åtgärd är det av vikt att veta om ett supra- eller infrainguinalt hinder föreligger i artärerna. En CI och samtidigt pulsbortfall i ljumsken är förenligt med aortoiliacala hinder, det vill säga suprainguinalt. Vid CI med bevarad ljumskpuls kan ett infrainguinalt hinder förmodas. Om det samtidigt finns ett blåsljud i ljumsken kan en multisegmentell ateroskleros misstänkas.
Rent allmänt är behandlingsresultaten efter intervention långsiktigt bättre inom högflödesområden (suprainguinalt) än i lågflödesområden (infrainguinalt). Därav de snävare indikationerna för kärlrekonstruktion vid infrainguinala stenoser/ocklusioner.
Interventionella behandlingsmetoder
Idag är till helt övervägande del endovaskulära kärlinterventioner aktuella vid CI. Vid suprainguinala hinder kan behandling ske på något vidare indikationer än vid infrainguinala hinder.
Via radiologisk intervention görs PTA (perkutan transluminal angioplastik – ”ballongvidgning”) av hindret. Oftast kombineras detta med inläggning av en eller flera stentar för att minska risken för ocklusion och restenos. Detta är ingrepp som görs i lokalanestesi under genomlysning.
Mera sällan kan det bli aktuellt med öppen kirurgi och då för anläggandet av extraanatomiska bypasser, exempelvis femoro-femoral bypass eller axillo-bifemoral bypass med syntetisk graft.
Även vid infrainguinala hinder är radiologisk intervention med PTA och stentning den dominerande metoden. Man kan idag stenta även underbensartärer. För att förbättra resultaten är läkemedelsfrigörande stentar under utveckling.
En variant av PTA är SAP – subintimal angioplastik. Detta innebär att interventionisten lägger katetern i gränsskiktet mellan intima och media och skapar ett nytt dissektionsplan i kärlet förbi stenosen/stenoserna och eventuella ocklusioner. Med ballongvidgningar i detta plan trycks den förtjockade intiman ihop tillsammans med ursprungligt kärllumen. På detta sätt skapas ett nytt lumen för blodet att flyta i. Metoden har sina svårigheter och begränsningar, men på många centra har den delvis ersatt konventionell bypasskirurgi.
Bypasskirurgi med öppen kirurgi görs endast undantagsvis vid CI, men är vanlig vid kritisk ischemi. Bypassen förbi den ockluderade delen av kärlet kan göras med patientens egen ven, så kallad autolog venbypass, antingen med reverserad ven (venen frias helt, tas ut och vändes därefter för att blodet inte ska stoppas av venklaffarna, varefter den anastomoseras med artären proximalt och distalt om hindret) eller med in-situteknik (venklaffarna destrueras med kateterteknik med venen på plats). Skulle det inte finnas någon användbar ven efter exempelvis tidigare varicerkirurgi eller koronarkirurgi, kan syntetiska grafter, kärlproteser, användas. Resultaten med syntetiska grafter är dock fortfarande betydligt sämre än vid användning av autolog ven.
Prognos
De flesta patienter med CI försämras inte utan har en i stort sett oförändrad klinisk bild (cirka 70–80 procent), åtminstone på medellång sikt (cirka fem år). I takt med progredierande ateroskleros försämras dock ofta besvären, eventuellt ända till kritisk ischemi (5–10 procent) och amputation (mindre än 2 procent).
Resultaten efter intervention varierar avsevärt med blodflödesområde och använd metod, men skiljer sig inte alltid så mycket från naturalförloppet på lite längre sikt, vilket är en information som är viktig att förmedla till patienten. Samtidigt är risken att få hjärtinfarkt eller stroke cirka 20 procent och mortaliteten cirka 10–15 procent efter fem år hos patienter med CI. Mortaliteten är till 75 procent relaterad till kardiovaskulära orsaker. Det är därför viktigt att förstå att CI inte är en godartad sjukdom, utan en indikator för en allvarlig systemsjukdom; generell ateroskleros.
Ovanstående siffror gäller även för den patient som ännu inte utvecklat subjektiva symtom, som CI, utan även den som enbart har ett ABI mindre än 0,9. Patienter med diabetes mellitus har generellt sämre prognos – man har talat om diabetessjukdomens aterosklerosaccellererande effekt.
Komplikationer
Komplikationerna är relaterade dels till grundsjukdomen (se under Prognos), dels till vald metod och indikation, varför exaktare siffror inte kan anges här. Rent allmänt gäller samma risk för komplikationer efter kärlingrepp som efter all annan kirurgi (blödning, infektion, ärrbildning, nervskador osv). Mera specifikt kan nämnas risken för pseudoaneurysm, ocklusion i stentade eller ballongvidgade kärlavsnitt samt risken för restenoser. Graftinfektion är en av de mer fruktade komplikationerna.
Särskilda och/eller förebyggande råd
CI bör uppfattas som ett symtom på en generell ateroskleros och profylax/behandling bör inrikta sig på detta. Riskfaktorsanering tillkommer en central betydelse och rökstopp är den enskilt viktigaste åtgärden.
Vidare information
Perifera artärsjukdomar i extremiteterna, Läkemedelsboken
Peripheral Arterial Occlusive Disease på emedicine
Bernartärsjukdom – Diagnostik och behandling, SBU
ICD-10
I70.2 - Ateroskleros i extremitetsartär
I73.9 - Perifer vaskulär sjukdom, ospecificerad
I73.9B - Claudicatio intermittens
Referenser
- SBU: Benartärsjukdom – diagnostik och behandling. Rapport 187:2007
- Läkemedelsboken 2011-2012 (under tryckning)
- Läkemedelsboken 2009-2010. 334-345: Perifera artärsjukdomar i extremiteterna.
- Koraen L, Wahlberg E. ABC om Claudicatio intermittens. Läkartidningen 2010;107;1774-1779